Peptidi su klasa spojeva nastalih povezivanjem više aminokiselina putem peptidnih veza.Oni su sveprisutni u živim organizmima.Do sada je u živim organizmima pronađeno na desetke tisuća peptida.Peptidi imaju važnu ulogu u regulaciji funkcionalnih aktivnosti različitih sustava, organa, tkiva i stanica te u životnim aktivnostima, a često se koriste u funkcionalnoj analizi, istraživanju antitijela, razvoju lijekova i drugim područjima.S razvojem biotehnologije i tehnologije sinteze peptida, sve više i više peptidnih lijekova se razvija i primjenjuje u klinici.
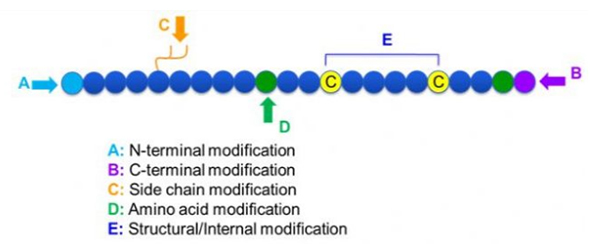
Postoji veliki izbor modifikacija peptida, koje se jednostavno mogu podijeliti na post modifikaciju i modifikaciju procesa (koristeći modifikaciju izvedenih aminokiselina), modifikaciju N-terminala, modifikaciju C-terminala, modifikaciju bočnog lanca, modifikaciju aminokiselina, modifikaciju kostura, itd., ovisno o mjestu modifikacije (slika 1).Kao važno sredstvo za promjenu strukture glavnog lanca ili skupina bočnih lanaca peptidnih lanaca, modifikacija peptida može učinkovito promijeniti fizikalna i kemijska svojstva peptidnih spojeva, povećati topljivost u vodi, produljiti vrijeme djelovanja in vivo, promijeniti njihovu biološku distribuciju, eliminirati imunogenost , smanjiti toksične nuspojave itd. U ovom radu predstavljeno je nekoliko glavnih strategija modifikacije peptida i njihovih karakteristika.
1. Ciklizacija
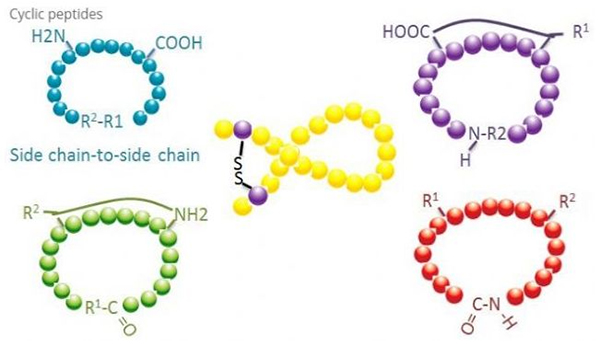
Ciklički peptidi imaju mnoge primjene u biomedicini, a mnogi prirodni peptidi s biološkom aktivnošću su ciklički peptidi.Budući da su ciklički peptidi čvršći od linearnih peptida, izuzetno su otporni na probavni sustav, mogu preživjeti u probavnom traktu i pokazuju jači afinitet za ciljne receptore.Ciklizacija je najizravniji način sintetiziranja cikličkih peptida, posebno za peptide s velikim strukturnim skeletom.Prema načinu ciklizacije, može se podijeliti na tip bočnog lanca bočnog lanca, tip terminala - bočnog lanca, tip terminala - terminala (tip s kraja na kraj).
(1) bočni lanac do bočnog lanca
Najčešći tip ciklizacije bočnog lanca u bočni lanac je disulfidni most između cisteinskih ostataka.Ova ciklizacija je uvedena tako što je par cisteinskih ostataka deprotektiran i zatim oksidiran da bi se formirale disulfidne veze.Policiklička sinteza može se postići selektivnim uklanjanjem sulfhidrilnih zaštitnih skupina.Ciklizacija se može izvesti ili u otapalu nakon disocijacije ili na smoli prije disocijacije.Ciklizacija na smolama može biti manje učinkovita od ciklizacije otapalom jer peptidi na smolama ne stvaraju lako ciklificirane konformacije.Druga vrsta ciklizacije bočnog lanca je stvaranje amidne strukture između ostatka asparaginske kiseline ili glutaminske kiseline i bazne aminokiseline, što zahtijeva da se zaštitna skupina bočnog lanca mora moći selektivno ukloniti iz polipeptida ili na smoli ili nakon disocijacije.Treći tip ciklizacije bočnog lanca - bočnog lanca je stvaranje difenil etera pomoću tirozina ili p-hidroksifenilglicina.Ova vrsta ciklizacije u prirodnim proizvodima nalazi se samo u mikrobnim proizvodima, a proizvodi ciklizacije često imaju potencijalnu medicinsku vrijednost.Priprema ovih spojeva zahtijeva jedinstvene reakcijske uvjete, tako da se ne koriste često u sintezi konvencionalnih peptida.
(2) terminal-bočni lanac
Ciklizacija krajnjeg bočnog lanca obično uključuje C-terminal s amino skupinom bočnog lanca lizina ili ornitina, ili N-terminal s bočnim lancem asparaginske kiseline ili glutaminske kiseline.Ostala ciklizacija polipeptida nastaje stvaranjem eterskih veza između terminala C i bočnih lanaca serina ili treonina.
(3) Terminalni ili tip od glave do repa
Lančani polipeptidi mogu se ciklirati u otapalu ili fiksirati na smolu cikliranjem bočnog lanca.U centralizaciji otapala treba koristiti niske koncentracije peptida kako bi se izbjegla oligomerizacija peptida.Prinos polipeptida sintetskog prstena od glave do repa ovisi o sekvenci polipeptidnog lanca.Stoga, prije pripreme cikličkih peptida u velikoj mjeri, najprije treba stvoriti biblioteku mogućih ulančanih vodećih peptida, nakon čega slijedi ciklizacija kako bi se pronašao slijed s najboljim rezultatima.
2. N-metilacija
N-metilacija se izvorno događa u prirodnim peptidima i uvodi se u sintezu peptida kako bi se spriječilo stvaranje vodikovih veza, čime se peptidi čine otpornijima na biorazgradnju i čišćenje.Sinteza peptida pomoću N-metiliranih derivata aminokiselina najvažnija je metoda.Dodatno, također se može koristiti Mitsunobu reakcija N-(2-nitrobenzen sulfonil klorid) polipeptid-smola međuprodukata s metanolom.Ova metoda je korištena za pripremu biblioteka cikličkih peptida koje sadrže N-metilirane aminokiseline.
3. Fosforilacija
Fosforilacija je jedna od najčešćih posttranslacijskih modifikacija u prirodi.U ljudskim stanicama više od 30% proteina je fosforilirano.Fosforilacija, posebno reverzibilna fosforilacija, igra važnu ulogu u kontroli mnogih staničnih procesa, kao što su prijenos signala, ekspresija gena, regulacija staničnog ciklusa i citoskeleta te apoptoza.
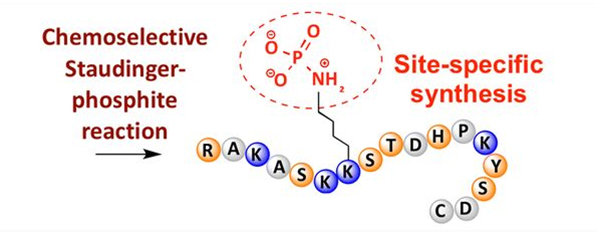
Fosforilacija se može uočiti na različitim aminokiselinskim ostacima, ali najčešći ciljevi fosforilacije su ostaci serina, treonina i tirozina.Derivati fosfotirozina, fosfotreonina i fosfoserina mogu se unijeti u peptide tijekom sinteze ili nastati nakon sinteze peptida.Selektivna fosforilacija može se postići korištenjem ostataka serina, treonina i tirozina koji selektivno uklanjaju zaštitne skupine.Neki reagensi za fosforilaciju također mogu uvesti skupine fosforne kiseline u polipeptid naknadnom modifikacijom.Posljednjih godina postignuta je fosforilacija lizina specifična za mjesto pomoću kemijski selektivne Staudinger-fosfitne reakcije (Slika 3).
4. Miristoilacija i palmitoilacija
Acilacija N-terminala s masnim kiselinama omogućuje peptidima ili proteinima da se vežu na stanične membrane.Miridamoilirana sekvenca na N-terminalu omogućuje protein kinazama obitelji Src i Gaq proteinima reverzne transkriptaze ciljano vezanje na stanične membrane.Miristinska kiselina je povezana na N-terminal polipeptida smole korištenjem standardnih reakcija spajanja, a rezultirajući lipopeptid se može disocirati pod standardnim uvjetima i pročistiti pomoću RP-HPLC.
5. Glikozilacija
Glikopeptidi poput vankomicina i teikolanina važni su antibiotici za liječenje bakterijskih infekcija otpornih na lijekove, a drugi glikopeptidi često se koriste za stimulaciju imunološkog sustava.Osim toga, budući da su mnogi mikrobni antigeni glikozilirani, od velike je važnosti proučavati glikopeptide za poboljšanje terapeutskog učinka infekcije.S druge strane, otkriveno je da proteini na staničnoj membrani tumorskih stanica pokazuju abnormalnu glikozilaciju, zbog čega glikopeptidi igraju važnu ulogu u istraživanju raka i imunološke obrane tumora.Glikopeptidi se pripremaju Fmoc/t-Bu metodom.Glikozilirani ostaci, kao što su treonin i serin, često se uvode u polipeptide pomoću fMOC-a aktiviranih pentafluorofenol esterom radi zaštite glikoziliranih aminokiselina.
6. Izopren
Izopentadienilacija se događa na cisteinskim ostacima u bočnom lancu blizu C-terminala.Proteinski izopren može poboljšati afinitet stanične membrane i stvoriti interakciju protein-protein.Izopentadijenirani proteini uključuju tirozin fosfatazu, malu GTazu, molekule kohaperona, nuklearnu laminu i centromerne vezne proteine.Izoprenski polipeptidi mogu se pripraviti korištenjem izoprena na smolama ili uvođenjem derivata cisteina.
7. Modifikacija polietilen glikola (PEG).
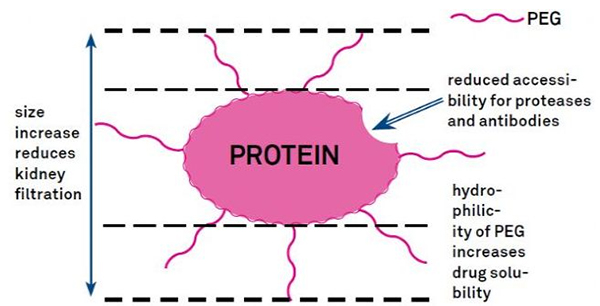
PEG modifikacija se može koristiti za poboljšanje hidrolitičke stabilnosti proteina, biodistribucije i topljivosti peptida.Uvođenje PEG lanaca u peptide može poboljšati njihova farmakološka svojstva i također inhibirati hidrolizu peptida proteolitičkim enzimima.Peptidi PEG prolaze kroz poprečni presjek glomerularnih kapilara lakše nego obični peptidi, znatno smanjujući bubrežni klirens.Zbog produljenog aktivnog poluživota PEG peptida in vivo, normalna razina liječenja može se održati nižim dozama i rjeđim peptidnim lijekovima.Međutim, PEG modifikacija ima i negativne učinke.Velike količine PEG-a sprječavaju enzim da razgradi peptid i također smanjuju vezanje peptida na ciljni receptor.No, nizak afinitet PEG peptida obično se nadoknađuje njihovim dužim farmakokinetičkim poluživotom, a budući da su dulje prisutni u tijelu, PEG peptidi imaju veću vjerojatnost da se apsorbiraju u ciljna tkiva.Stoga bi specifikacije PEG polimera trebale biti optimizirane za optimalne rezultate.S druge strane, PEG peptidi se nakupljaju u jetri zbog smanjenog bubrežnog klirensa, što rezultira makromolekularnim sindromom.Stoga se PEG modifikacije moraju pažljivije dizajnirati kada se peptidi koriste za testiranje lijekova.
Uobičajene modifikacijske skupine PEG modifikatora mogu se ugrubo sažeti kako slijedi: amino (-amin) -NH2, aminometil-Ch2-NH2, hidroksi-OH, karboksi-Cooh, sulfhidril (-tiol) -SH, maleimid -MAL, sukcinimid karbonat - SC, sukcinimid acetat -SCM, sukcinimid propionat -SPA, n-hidroksisukcinimid -NHS, akrilat-ch2ch2cooh, aldehid -CHO (kao što je propional-ald, butyrALD), akrilna baza (-akrilat-acrl), azido-azid, biotinil - Biotin, fluorescein, glutaril -GA, akrilat hidrazid, alkin-alkin, p-toluensulfonat -OTs, sukcinimid sukcinat -SS, itd. PEG derivati s karboksilnim kiselinama mogu se vezati na n-terminalne amine ili lizinske bočne lance.Amino-aktivirani PEG može se spojiti na bočne lance asparaginske kiseline ili glutaminske kiseline.Loše aktivirani PEG može se konjugirati u merkaptan potpuno deprotektiranih bočnih lanaca cisteina [11].PEG modifikatori se obično klasificiraju kako slijedi (napomena: mPEG je metoksi-PEG, CH3O-(CH2CH2O)n-CH2CH2-OH):
(1) ravnolančani PEG modifikator
mPEG-SC, mPEG-SCM, mPEG-SPA, mPEG-OTs, mPEG-SH, mPEG-ALD, mPEG-butyrALD, mPEG-SS
(2) bifunkcionalni PEG modifikator
HCOO-PEG-COOH, NH2-PEG-NH2, OH-PEG-COOH, OH-PEG-NH2, HCl·NH2-PEG-COOH, MAL-PEG-NHS
(3) modifikator grananja PEG
(mPEG)2-NHS, (mPEG)2-ALD, (mPEG)2-NH2, (mPEG)2-MAL
8. Biotinizacija
Biotin se može snažno vezati s avidinom ili streptavidinom, a snaga vezanja je čak blizu kovalentne veze.Peptidi obilježeni biotinom obično se koriste u imunotestovima, histocitokemiji i protočnoj citometriji temeljenoj na fluorescenciji.Označena antitijela na antibiotik također se mogu koristiti za vezanje biotiniliranih peptida.Biotinske oznake često su pričvršćene na bočni lanac lizina ili N terminal.6-aminokapronska kiselina često se koristi kao veza između peptida i biotina.Veza je fleksibilna u vezivanju za supstrat i bolje se veže u prisutnosti steričke smetnje.
9. Fluorescentno označavanje
Fluorescentno označavanje može se koristiti za praćenje polipeptida u živim stanicama i proučavanje enzima i mehanizama djelovanja.Triptofan (Trp) je fluorescentan, pa se može koristiti za intrinzično označavanje.Spektar emisije triptofana ovisi o perifernom okruženju i smanjuje se sa smanjenjem polariteta otapala, što je svojstvo koje je korisno za otkrivanje strukture peptida i vezanja receptora.Fluorescencija triptofana može se ugasiti protoniranom asparaginskom kiselinom i glutaminskom kiselinom, što može ograničiti njegovu upotrebu.Dansil kloridna skupina (Dansyl) vrlo je fluorescentna kada je vezana za amino skupinu i često se koristi kao fluorescentna oznaka za aminokiseline ili proteine.
Fluorescencijska rezonancija Pretvorba energije (FRET) korisna je za studije enzima.Kada se primjenjuje FRET, supstratni polipeptid obično sadrži skupinu za označavanje fluorescencije i skupinu za gašenje fluorescencije.Označene fluorescentne skupine prigušuje prigušivač nefotonskim prijenosom energije.Kada se peptid odvoji od dotičnog enzima, skupina za označavanje emitira fluorescenciju.
10. Kavezni polipeptidi
Kavezni peptidi imaju optički uklonjive zaštitne skupine koje štite peptid od vezanja na receptor.Kada je izložen UV zračenju, peptid se aktivira, vraćajući svoj afinitet prema receptoru.Budući da se ova optička aktivacija može kontrolirati prema vremenu, amplitudi ili lokaciji, kavezni peptidi mogu se koristiti za proučavanje reakcija koje se odvijaju u stanicama.Najčešće korištene zaštitne skupine za polipeptide kaveza su 2-nitrobenzilne skupine i njihovi derivati, koji se mogu uvesti u sintezu peptida putem zaštitnih derivata aminokiselina.Razvijeni derivati aminokiselina su lizin, cistein, serin i tirozin.Međutim, derivati aspartata i glutamata nisu često korišteni zbog njihove osjetljivosti na ciklizaciju tijekom sinteze i disocijacije peptida.
11. Poliantigeni peptid (MAP)
Kratki peptidi obično nisu imuni i moraju se spojiti na proteine nosače da bi proizveli antitijela.Poliantigenski peptid (MAP) sastoji se od višestrukih identičnih peptida povezanih s jezgrama lizina, koji mogu specifično eksprimirati imunogene visoke potencije i mogu se koristiti za pripremu spojeva proteina peptid-nosač.MAP polipeptidi mogu se sintetizirati sintezom čvrste faze na MAP smoli.Međutim, nepotpuno spajanje rezultira nedostatkom ili skraćenim peptidnim lancima na nekim granama i stoga ne pokazuje svojstva originalnog MAP polipeptida.Kao alternativa, peptidi se mogu pripremiti i pročistiti odvojeno i zatim spojiti na MAP.Peptidna sekvenca vezana za peptidnu jezgru dobro je definirana i lako se karakterizira masenom spektrometrijom.
Zaključak
Modifikacija peptida je važan način dizajniranja peptida.Kemijski modificirani peptidi ne samo da mogu održati visoku biološku aktivnost, već i učinkovito izbjeći nedostatke imunogenosti i toksičnosti.U isto vrijeme, kemijska modifikacija može peptidima dati neka nova izvrsna svojstva.Posljednjih godina ubrzano se razvija metoda CH aktivacije za postmodifikaciju polipeptida, te su postignuti mnogi važni rezultati.
Vrijeme objave: 20. ožujka 2023
